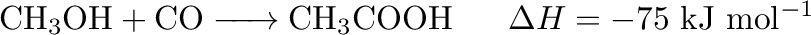 |
(9.3) |
Az ecetsav általános jelentőségét szükségtelen kidomborítani9.1. Az előállításával kapcsolatban a legtöbb embernek a biológiai fermentáció jut eszébe, és ha az élelmiszeripart tekintjük, nem is alaptalanul. A teljes ecetsav mennyíség kb. 75%-át azonban metanol katalitikus karbonilezésével állítják elő. Sztenderd körülmények között a reakció termodinamikailag kényelmesen engedélyezett:
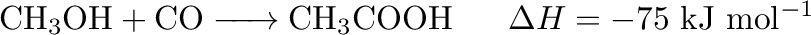 |
(9.3) |
![$\displaystyle \ce{RhI3 + 3 CO + H2O -> H+ + [Rh(CO)2I2]- + CO2 + HI}$](img224.png) |
(9.4) |
A Monsanto-eljáráshoz 30 bar CO nyomás és 150 hőmérséklet szükségeltetik, de néha ennél magasabb értékek is előfordulnak. A reakció mechanizmusát a 9.13 ábra mutatja be. A teljes folyamat felbontható egy katalitikus és egy nemkatalitikus körfolyamatra. Az utóbbi tartalmazza a metanol reakcióját hidrogén jodiddal, valamint a keletkező termék (acetil-jodid) hidrolízisét ecetsavvá.
A reakció a metil-jodid oxidatív addíciójával kezdődik (1). Kinetikai kísérletek és elméleti számítások egyaránt azt valószínűsítették, hogy itt nem a “hagyományos” addícióról van szó a telítetlen fémkomplex és a metil-jodid egyídejű kapcsolódásával a ródiumhoz. A részlépés ehelyett SN2 mechanizmussal megy végbe, ahol a fémtartalmú anion tölti be a nukleofil ágens szerepét. A metilszén-ródium kötés kialakulását követően a metil-jodidból származó jodidion megtalálja az útját a maradék üres koordinációs helyen, azaz a metil csoporthoz képest transz pozícióban. Kinetikai mérések azt is megerősítették, hogy az SN2 reakció a sebességmeghatározó lépés a ciklusban.
Az oktaéderes komplex ezt követően vándorlásos beékelődéssel tetragonális piramis szerkezetűvé alakul át az acetil csoport kialakulása mellett (2). A külső gáztérből érkező CO viszont a felszabaduló axiális helyet foglalja el, így a fac-cisz izomer keletkezik (3). (Igazság szerint ez az izomer verseng a stabilisabb mer-transz izomerrel, annál azonban a reduktív elimináció lassabban megy végbe.) Az acetil ligandum ezután az egyik axiális jodido ligandummal kapcsolódik össze és reduktív eliminációval visszaadja a cisz-[RhI2(CO)2]- komplexet (4), emellett keletkezik az acetil-jodid termék. A jelenlevő víz hatására a CH3I elhidrolizál ecetsav végterméket és hidrogén jodidot eredményezve. A reakció végén az ecetsavat desztillációval különítik el.
A Cativa eljárás attraktívabb két okból is. Egyrészt az ennél alkalmazott iridium olcsóbb, mint a ródium (és ami a pénzügyi tervezésnél fontos, az ára kisebb volatilitást is mutat), másrészt az alkalmazott reakciókörülmények is enyhébbek, és a reakció kb. 25%-kal gyorsabb, mint a Monsanto szintézis. A mechanizmus szinte ugyanaz ebben az esetben is, kis különbséggel. Az [IrI2(CO)3(CH3)]- komplexnél ugyanis a CO beékelődés a [IrI3(CO)2(CH3)]- komplexhez képest gyorsabban megy végbe. A kétféle lehetséges szén-monoxid beékelődést a 9.14 ábra mutatja be.
A trikarbonil komplex képződését kokatalizátorral segítik elő. A Cativa eljárásnál a feltételezések szerint már nem az oxidatív addíció, hanem a beékelődés a sebességmeghatározó, így ez az a pont, ahol a promotor hatása lényeges lehet. A BP által alkalmazott eljárásnál Ru-karbonil (egész pontosan Ru(CO)4I2) komplexből jön létre a jodid só a reakciókörülmények közepette, de szoktak közvetlenül fém-jodidokat is alkalmazni.
A Monsanto-eljárás egy speciális válfaja az ecetsavanhidrid előállítására használt Eastman-eljárás. A különbségek abból adódnak, hogy az anhidrid előállítás termodinamikája sokkal közelebb van az egyensúlyihoz:
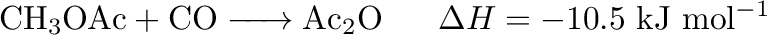 |
(9.5) |
A só adalékok hatása nem teljesen tisztázott, viszont megfigyelték, hogy a reakció a leggyakrabban alkalmazott kation, a lítium esetében elsőrendű és nagy Li+ koncentráció jelentős sebességnövekedést eredményez. Az Eastman-eljárás szerves ciklusa a 9.15 ábrán látható.