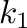 és
és  sebességi állandókkal jellemezhetjük.
sebességi állandókkal jellemezhetjük.
A katalitikus ciklusok jellemzően több lépésből állnak, így a konszekutív modell (ha sokszor túlzott leegyszerűsítést is jelent) alkalmazható. A 4.16 egyenlet a legegyszerűbb esetet vázolja fel, amikor is a kiindulási anyagból (A) egy köztitermék (B) keletkezik, majd abból a termék (C). A két részlépést 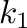 és
és  sebességi állandókkal jellemezhetjük.
sebességi állandókkal jellemezhetjük.
Kezdeti feltételként (ha  ), rögzíthetjük, hogy
), rögzíthetjük, hogy
![$[\mathrm{A}]=[\mathrm{A}]_0$](img101.png) ,
,
![$[\mathrm{B}]=[\mathrm{C}]=0$](img102.png) . A differenciálegyenlet-rendszer megoldása és a behelyettesítések után a három anyag koncentrációjára az alábbi egyenleteket kapjuk:
. A differenciálegyenlet-rendszer megoldása és a behelyettesítések után a három anyag koncentrációjára az alábbi egyenleteket kapjuk:
![\begin{equation*}\left.\begin{aligned}[\mathrm{A}]&=[\mathrm{A}]_0e^{-k_1t} \\
...
...0}{k_2-k_1}(-k_2e^{-k_1t}+k_1e^{-k_2t})\end{aligned}\right\rbrace\end{equation*}](img103.png) |
Ha a reakciónkhoz még egy további lépést hozzáadunk, akkor már három sebességi állandóval kell számolnunk:
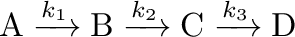 |
(4.18) |
![\includegraphics[width=0.99\textwidth]{kinetika/abcd_peldak}](img105.png)
|
A négyismeretlenes közönséges differenciálegyenlet-rendszer megoldása (itt nem részletezett módon) numerikusan történt, a négy komponens koncentrációjának időfüggése a 4.2 ábrán látható. A két koncentráció-idő profil összehasonlítása egy fontos jelenségre hívja fel figyelmünket, mely alapvető korlátot jelent bizonyos reakciók intermedierjeinek kísérleti úton történő tanulmányozásához. Ha ugyanis az utolsó részlépés a sebességmeghatározó, akkor elvileg a reakció intermedierjeit spektroszkópiai úton be lehet azonosítani. Ha azonban az első két lépés valamelyike a sebességmeghatározó lépés, akkor az “leárnyékolja” az összes többit. Az alsó példánál a B
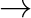 C lépés jóval lassabb, mint a zárólépés, így C intermediert gyakorlatilag nem látjuk az oldatban annak igen kis koncentrációja miatt.
C lépés jóval lassabb, mint a zárólépés, így C intermediert gyakorlatilag nem látjuk az oldatban annak igen kis koncentrációja miatt.