![\includegraphics[width=0.9\textwidth]{elemi/ptioncoinz}](img123.png)
|
A vándorlásos beékelődés azt a folyamatot írja le, amikor egy telítetlen molekula egy fém-ligandum (jellemzően anionos ligandum) kötésbe lép be. A 5.4 ábrán bemutatott Pt(II) komplexben a cisz helyzetben levő CO- és metilcsoport kapcsolódik össze egy acetil csoporttá egy háromcentrumos átmeneti állapoton keresztül, majd az üres koordinációs helyet a triklorosztannát anion tölti be. Az átmeneti állapot feltételezett geometriáját elméleti számítások is megerősítették.
Noha a reakciót szoktuk röviden beékelődésnek, vagy inzerciónak is hívni, itt nem a CO ékelődik be közvetlenül a fém és a metil szén közé, hanem a metilcsoport (illetve általánosan az alkil csopoort) parciális negatív töltéssel rendelkező szénatomja keresi meg magának az utat a karbonil ligandum parciális pozitív töltésű szénatomjához ([1, 1]-beékelődés).
Eddig feltételeztük, hogy a reagáló szén-monoxid a fémhez koordinálódik. Kísérleti bizonyítékok alapján a metilvándorlás valóban a koordinált CO-ra történik. A klasszikus bizonyíték egy viszonylag inert komplexből származik, ahol mind a vándorlás, mind a koordinált CO cseréje lassú. Amikor a CH3Mn(CO)5 továbbreagál 13C-mal jelzett szabad CO jelenlétében, a keletkező CH3(CO)Mn(CO)4(13CO) termékben a jelzett CO koordinált formában, nem pedig az acetilcsoportban van jelen. Ezért nincs közvetlen reakció a metil-mangán egység és az újonnan érkező szén-monoxid között (5.5 ábra).
Termodinamikai oka is van annak, hogy ez előbbi esetben és az esetek nagy részében miért az intramolekuláris beékelődés a kedvezményezett a külső gáztérből érkező szén-monoxiddal szemben. Az addícionáló CO entrópiacsökkenéssel jár, míg ha már a koordinált karbonil ligandum lép reakcióba, akkor általában nem számolhatunk jelentős entrópiaváltozással. Így a 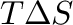 tag akkor is megnöveli az aktiválási szabadentalpiát, ha a két folyamatra az aktiválási entalpia ugyanannyi.
tag akkor is megnöveli az aktiválási szabadentalpiát, ha a két folyamatra az aktiválási entalpia ugyanannyi.
A vándorlásos beékelődés egy másik fontos válfaja elsősorban az alkénekkel kapcsolatos. A 5.6 ábra egy hidrid ligandum vándorlását mutatja egy koordinált etén molekulához, mely a hidridhez képest cisz-pozícióban van. A hidridvándorlás egy üres helyet eredményez a fém koordinációs övezetében, azaz a koordinációs szám eggyel csökken. Ezt az üres helyet két módon lehet kitölteni: először agosztikus kölcsönhatás lép fel a 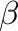 -hidrogénekkel, második lépésben egy új ligandum elfoglalhatja a szabad helyet. A feltételezett mechanizumst, melyet [1, 2]-beékelődésnek is szoktak nevezni, számos elméleti és kísérleti munka is alátámasztotta. Az átmeneti állapotot megfigyelve látszik némi hasonlóság a [2+2] cikloaddíciós reakciókkal.
-hidrogénekkel, második lépésben egy új ligandum elfoglalhatja a szabad helyet. A feltételezett mechanizumst, melyet [1, 2]-beékelődésnek is szoktak nevezni, számos elméleti és kísérleti munka is alátámasztotta. Az átmeneti állapotot megfigyelve látszik némi hasonlóság a [2+2] cikloaddíciós reakciókkal.
Nem mindig egyértelmű, hogy egy koordinált alkén hogyan aktiválódik vándorlás előtt. A koordinált alkének hajlamosak 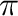 -viszontkoordinációra és
-viszontkoordinációra és 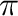 -donor kölcsönhatásra, és ezekből az összhatás nem mindig megjósolható. Elektronszerkezeti számítások gyakran azt mutatják, hogy a koordinált alkén nem aktiválódik a vándorlás irányába, és nem lehet előre megjósolni, hogy a hidrid gyors vándorlása bekövetkezik-e. Az erős viszontkoordináció miatt például az elektronokban gazdagabb alkének kevésbé érzékenyek a nukleofil csoportok, így a hidrid támadására.
-donor kölcsönhatásra, és ezekből az összhatás nem mindig megjósolható. Elektronszerkezeti számítások gyakran azt mutatják, hogy a koordinált alkén nem aktiválódik a vándorlás irányába, és nem lehet előre megjósolni, hogy a hidrid gyors vándorlása bekövetkezik-e. Az erős viszontkoordináció miatt például az elektronokban gazdagabb alkének kevésbé érzékenyek a nukleofil csoportok, így a hidrid támadására.
Az alkén polimerizációs reakciók esetén a jellemző lépés az olefininzerció a fém és a rajta már meglévő alkillánc közé. Ha a fém-alkil kötésbe történő beékelődéseket összehasonlítjuk, akkor termodinamikailag az alkének beékelődése egy fém-alkil kötésbe sokkal kedvezőbb, mint a szén-monoxid beékelődése. Az utóbbi reakció termoneutrális, vagy enyhén exergonikus, és az egyensúlyi állandó standard körülmények között közel egyensúlyt mutat. Az alkének beékelődése a fém-szén kötésbe energetikailag kedvező és általában irreverzibilis (Ha nem az, akkor nincs jelentős láncnövekedés!). Az energianyereség nagysága körülbelül 80 kJ/mol, amikor egy alkén kettős kötéséből egyes kötés lesz, egy új egyes kötés kialakulása mellett. A fém-hidrid kötés viszont erősebb, mint a fém-szén kötés, és a szén-monoxid beékelődése egy fém-hidrid kötésbe termodinamikailag többnyire kedvezőtlen. Az alkén beékelődése egy fém-hidridbe termodinamikailag megengedett és gyakran reverzibilis, sőt, néha az egyensúly az alkil komplexek irányába tolódik el. A beékelődés során a vegyértékelektronok száma kettővel, a koordinációs szám eggyel csökken, a fém oxidációs száma nem változik.
A vándorlásos beékelődési reackió fordítottját, amikor a fém-alkil komplex alakul át alkén-hidrid komplexszé, 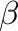 -eliminációnak nevezzük.
A
-eliminációnak nevezzük.
A 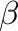 -elimináció a komplex elektronszámát kettővel növeli. A koordinációs szám eggyel nő, így a
-elimináció a komplex elektronszámát kettővel növeli. A koordinációs szám eggyel nő, így a 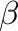 -eliminációhoz szükséges egy szabad hely (a koordinált oldószermolekulák kivételével) a komplexben. A reakcióban komoly szerepe van az agosztikus kölcsönhatásnak, mely az a lépés, ahol a fém “felveszi a kapcsolatot” a
-eliminációhoz szükséges egy szabad hely (a koordinált oldószermolekulák kivételével) a komplexben. A reakcióban komoly szerepe van az agosztikus kölcsönhatásnak, mely az a lépés, ahol a fém “felveszi a kapcsolatot” a 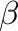 -szénatomon levő hidrogénnel (lásd 5.6 ábra, ha fordított irányban tekintünk a folyamatokra).
-szénatomon levő hidrogénnel (lásd 5.6 ábra, ha fordított irányban tekintünk a folyamatokra).
A 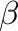 -elimináció meggátolja erőfeszítéseinket, ha alkil komplexeket szeretnénk előállítani, és visszadob minket a kezdőpontra, ha pl. olefin hidrogénezésről, vagy hidroformilezésről van szó. Gátlása ezért gyakran kívánatos lenne, és többféle módon el is érhető:
-elimináció meggátolja erőfeszítéseinket, ha alkil komplexeket szeretnénk előállítani, és visszadob minket a kezdőpontra, ha pl. olefin hidrogénezésről, vagy hidroformilezésről van szó. Gátlása ezért gyakran kívánatos lenne, és többféle módon el is érhető:
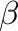 -hidrogén, akkor nincs
-hidrogén, akkor nincs 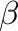 -elimináció sem. Ilyen alkil csoport lehet pl. a metil, neopentil, vagy trimetil-szilil.
-elimináció sem. Ilyen alkil csoport lehet pl. a metil, neopentil, vagy trimetil-szilil.
A deinzerció és extrúzió kifejezéseket gyakran használják a 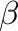 -elimináció helyett, különösen CO esetén. Mindkét folyamat üres koordinációs helyet igényel, és a fém vegyértékelektronjainak száma kettővel nő a deinzerció során (feltéve, hogy a CO koordinálva marad). A deinzercióhoz egy üres koordinációs helyre is szükség van az acil csoport cisz pozíciójában.
-elimináció helyett, különösen CO esetén. Mindkét folyamat üres koordinációs helyet igényel, és a fém vegyértékelektronjainak száma kettővel nő a deinzerció során (feltéve, hogy a CO koordinálva marad). A deinzercióhoz egy üres koordinációs helyre is szükség van az acil csoport cisz pozíciójában.