![\includegraphics[width=0.67\textwidth]{karbonil/hydroalk_eq}](img206.png)
|
Ezen reakciók mindegyike leírható egy olyan általános sémával (9.1 ábra), melyben az olefinre formálisan egy szén-monoxid és egy hidrogénforrásként szolgáló H-X vegyület addiciónálódik. A hidroformilezés esetében X=H; ha X=OH, azaz a hidrogénforrásunk víz, akkor hidrokarboxilezésről; ha X=OR, azaz a szubsztrátum észter, akkor hidroalkoxikarbonilezésről beszélünk. Utóbbi reakciót a szakirodalomban hidroészterezésnek is nevezik. Noha komolyabb áttörést az iparban még egyik reakció sem ért el, az olefin karbonilezésével előállítható karbonsavak, illetve észterek nagy érdeklődésre tarthatnak számot.
A reakció mechanizmusa akár bonyolultnak is mondható, ugyanis a legtöbb reakciónál megszokott körfolyamat helyett itt két, egymással összedolgozó katalitikus ciklus van (9.2 ábra). Godard et al. [2008], Guiu et al. [2006], Cavinato and Toniolo [1990] A hidrides mechanizmus analógnak tekinthető a Co/Rh/Pt-Sn mechanizmusokkal, azaz a palládium-hidrid komplex olefin beékelődéssel alkil komplexekhez vezet (1). A külső gáztérből egy szén-monoxid érkezik; a CO beékelődést követően acil komplexet kapunk (2). Az alkohol oxidatív addícióját és az észter termék reduktív eliminációját követően visszakapjuk a hidrid komplexet (3).
Az alkoxi ciklusban az alkoxi-palládium komplexre koordinálódik egy szén-monoxid molekula, majd végbemegy a CO beékelődése (4). Ezt követi az alkén koordinációja, majd beékelődése a Pd-O kötésbe (5). A folyamatot itt is az alkohol oxidatív addíciója, majd a termék reduktív eliminációja zárja (4). Általában elfogadott, hogy mindkét ciklusnál az alkoholízis, tehát a zárólépés a sebességmeghatározó.
![\includegraphics[width=1.02\textwidth]{karbonil/hidroalkoxikarb_mech}](img207.png)
|
A két ciklus megléte a gyanútlan szemlélődőben felveti a “tyúk, vagy a tojás” problémáját. Hidroformilezésnél egyszerű a kép a katalizátor kialakulását illetőleg: a prekurzor komplex reagál a molekuláris dihidrogénnel és fém-hidrid keletkezik (a klórtartalmú prekurzor esetén HCl eliminációval kísérve). A feltételezések szerint itt is hasonló dolog történik: a PdL2Cl2 komplex alkoholízise szintén HCl eliminációval jár együtt és az alkoxi-komplexet eredményezi, ami a tulajdonképpeni katalizátor az alkoxi ciklusban. Ez még nem magyarázná meg, hogyan jutunk el a hidrid ciklusig, ám ha megnézzük, milyen termék keletkezik az alkoxi ciklusban az alkén beékelődést követően, akkor láthatjuk, hogy itt egy alkil komplexről van szó, mely tartalmaz 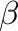 -hidrogént! A
-hidrogént! A 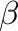 -elimináció már megmagyarázza, hogyan lehet hidridünk, amit az acil komplexből az alkoholízis után vissza is kapunk. Ha viszont az alkoxi mechanizmus alkoxikarbonil-alkil komplexe reagál alkohollal, akkor (a termék képződése mellett) az alkoxi komplexet kapjuk meg.
-elimináció már megmagyarázza, hogyan lehet hidridünk, amit az acil komplexből az alkoholízis után vissza is kapunk. Ha viszont az alkoxi mechanizmus alkoxikarbonil-alkil komplexe reagál alkohollal, akkor (a termék képződése mellett) az alkoxi komplexet kapjuk meg.
A feltételezések szerint a regioszelektivitást jórészt az szabja meg, hogy a két ciklus közül melyik dominál. Sztirol szubsztrátum esetén pédául a Pd-alkoxikarbonil kötésbe az elágazó, míg a Pd-H kötésbe a lineáris sztirol beékelődés a preferált. Magától értetődő, hogy a ligandumok szerepe igen fontos a kívánt lineáris/elágazó arány elérésében. Monofoszfinok jellemzően elágazó, míg a difoszfinok (mint a dppp) lineáris észterekhez vezetnek.
A hidroalkoxikarbonilezés alkalmas módszernek ígérkezik királis észterek előállítására is, és ebből a szempontból nézve a megfelelő enantioszelektivitás mellett nagyon fontos a nagy elágazó regioszelektivitás is. Noha ezek eredete még nincs teljesen tisztázva, néhány olyan megfigyelés történt, amik figyelembe vételével a szelektivitás szisztematikus növelésére van lehetőség.
Az egyfogú ligandumok cisz/transz-izomériára képesek; néhány közlemény szerint ez egyes esetekben növelheti az elágazó termékek arányát. Ennél kézzelfoghatób eredmények születtek a difoszfinok kelátszögeivel kapcsolatban. Ha 1,3-difenilfoszfino-propán (dppp) helyett az amúgy ritkán használt 1,6-difenilfoszfino-hexánt alkalmazzuk, akkor az elágazó regioszelektivitás a monofoszfinokkal kapott eredményekhez hasonlóan alakul. A difoszfinokon az elektronszívó szubsztituensek jelenléte szintén jelentősen képes javítani a regioszelektivitást. Ha például a DIOP ligandum 3,5-pozícióban trifluormetil csoportokat tartalmaz, akkor a regioszelektivitás 51%-ról 92%-ra nőtt. (Ezzel szemben viszont sajnos csökkent az enantioszelektivitás.) A nagy kelátszög mellett a jelentősebb sztérikus gátlás is az elágazó észterek keletkezésének kedvez.
Feltételezések szerint az elektronikus hatások ligandumon keresztül történő variálása egyes intermedierek stabilizálásához vezet. Ha mondjuk a hidrides ciklusban az elágazó alkil komplexek stabilitását növelni lehet egy  -jellegű koordinációval, az növelni fogja az elágazó közti termékek arányát a körfolyamat során. (Ha az alkén beékelődés lenne a sebességmeghatározó és nem az alkoholízis, akkor ennek nem lenne jelentősége, mivel a lassú lépésben eldőlne a regioizomerek aránya.)
-jellegű koordinációval, az növelni fogja az elágazó közti termékek arányát a körfolyamat során. (Ha az alkén beékelődés lenne a sebességmeghatározó és nem az alkoholízis, akkor ennek nem lenne jelentősége, mivel a lassú lépésben eldőlne a regioizomerek aránya.)
![\includegraphics[width=0.8\textwidth]{karbonil/pdintermstabil}](img208.png)
|
A másik stabilizáló jellegű kölcsönhatás is a hidrid ciklusban fordul elő. Difoszfinok esetében valószínűsíthető, hogy  -acil intermedier alakul ki a CO beékelődés után, ami növeli az alkoholízis sebességét. Ha ez nagyobb arányban jön létre az elágazó acil komplexek esetében, akkor az elágazó termékek aránya is nagyobb lesz. A Pd-alkil és Pd-acil intermedierek stabilizáló jellegű kölcsönhatásait a 9.3 ábra mutatja be.
-acil intermedier alakul ki a CO beékelődés után, ami növeli az alkoholízis sebességét. Ha ez nagyobb arányban jön létre az elágazó acil komplexek esetében, akkor az elágazó termékek aránya is nagyobb lesz. A Pd-alkil és Pd-acil intermedierek stabilizáló jellegű kölcsönhatásait a 9.3 ábra mutatja be.